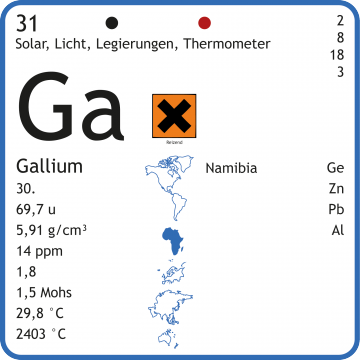
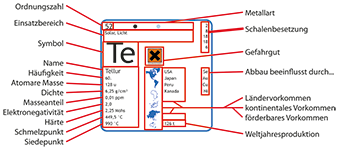
Gallium-Chemie
Nachweis
Eine gute Vorprobe für Gallium ist ein Versuch, bei dem die Boraxperle verwendet wird.
Zuerst glüht man ein Magnesiastäbchen solange aus, bis die Manganeigene charakteristische Eigenfärbung in der Flamme verschwunden ist. Daraufhin nimmt man mit dem Magnesiastäbchen Borax auf und schmilzt dieses Salz in der Flamme des Brenners zu einer glasklaren Perle.
Während diesem Vorgang entweicht das Kristallwasser.
Mit der Perle nimmt man anschließend ein…
» Lesen Sie mehr…

Darstellung
Gallium wird als Nebenprodukt bei der Aluminiumherstellung aus Bauxit im Bayer-Verfahren gewonnen. Als Ausgangsprodukt dient das dabei in Natronlauge gelöste Gemisch von Natriumaluminat und Natriumgallat. Durch verschiedene Verfahren kann hieraus Gallium vom Aluminium getrennt werden. Eine Möglichkeit ist die fraktionierte Kristallisation mit Hilfe von Kohlenstoffdioxid, wobei zunächst bevorzugt Aluminiumhydroxid ausfällt, während sich das leichter lösliche Natriumg…
» Lesen Sie mehr…

Eigenschaften
Gallium ist ein silberweißes, weiches (Mohs-Härte: 1,5) Metall. Es hat einen für Metalle ungewöhnlich niedrigen Schmelzpunkt, der bei 29,76 °C liegt. Es ist damit nach Quecksilber und Caesium das Metall mit dem niedrigsten Schmelzpunkt, der auch deutlich unter denjenigen der benachbarten Elemente Aluminium und Indium liegt. Verantwortlich hierfür ist wahrscheinlich die ungewöhnliche Kristallstruktur, die im Gegensatz zu den Strukturen anderer Metalle keine…
» Lesen Sie mehr…

Verbindungen
Gallium kommt in Verbindungen fast ausschließlich in der Oxidationsstufe +3 vor. Daneben sind seltene und meist sehr instabile Gallium(I)-Verbindungen bekannt sowie solche, die sowohl ein- als auch dreiwertiges Gallium enthalten (formal Gallium(II)-Verbindungen).
Verbindungen mit Elementen der Stickstoffgruppe
Die technisch wichtigsten Verbindungen des Galliums sind diejenigen mit den Elementen der Stickstoffgruppe. Galliumnitrid, Galliumphosphid, Galliumarsenid und Galliumantimonid sind…
» Lesen Sie mehr…